鹅细小病毒与鸭圆环病毒混合感染对鸭的影响
日期:2025-07-31 来源: 鸭高创咨询公众号
- 字号:
- [大]
- [中]
- [小]
鹅细小病毒(GPV)可引起番鸭幼雏和雏鹅患上小鹅瘟,发病率和死亡率较高。该病毒可引起厌食、水样腹泻和发育迟缓。感染后不到一周的雏鹅死亡率高达100%。此外,GPV还可引起短喙侏儒综合征(SBDS),该综合征于1971年在法国的骡鸭群中首次报道。SBDS的临床症状是生长迟缓、舌头突出和胫骨短而粗,其特点是发病率和死亡率较低。自2015年以来,有报道称GPV导致中国樱桃谷鸭患上SBDS。
鸭圆环病毒 (DuCV) 属于圆环病毒科圆环病毒属,最初报道于德国一家农场的两只6周龄雌性骡鸭中;两只鸭均出现羽毛脱落异常且身体状况不佳。DuCV感染可能使宿主易患免疫抑制,而与其他细菌和病毒病原体的共同感染会进一步加剧病情进展。例如,一项研究发现,感染 DuCV 的鸭更容易感染鸭疫里默氏杆菌、大肠杆菌、鸭肝炎病毒1型。由于缺乏用于病毒扩繁的细胞培养系统,因此人们对DuCV的分子生物学和发病机制知之甚少。为了明确表征与 DuCV 感染相关的疾病,需要合适的动物模型。
流行病学调查显示,SBDS中存在的GPV和DuCV在中国东部地区鸭群中很常见,鸭群中SBDS的致病性已得到证实。尽管GPV已被证实为鸭SBDS的病原体,但该病很少通过实验感染再现。尚不清楚DuCV 是否与 GPV 产生协同作用,并影响两种病毒的复制和致病性。
在本文中研究人员通过建立肉鸭的共感染模型,并评估了病毒在鸭中的复制和致病性,以了解 GPV 和 DuCV 之间的协同作用。
研究人员将60只2日龄雏鸭分成4组。鸭子腹腔接种方法见表1。对照组不予治疗。感染后10、20、30天(即10dpi、20dpi、30dpi),每组随机选取3只鸭子处死,取组织样本进行组织病理学(肝脏、肾脏、十二指肠、脾脏、胸腺、法氏囊和骨髓)、免疫组化及病毒载量分析(心脏、肝脏、肺脏、肾脏、十二指肠、脾脏、胸腺、法氏囊和骨髓)。感染后每5天测量一次体重。
2. 试验结果
2.1 体重和肉眼病变
两种病毒都对鸭子生长性能造成不同程度的影响,导致生长迟缓和体重增加较差,以至于鸭子的体重仅为无病毒鸭子的60%。从10dpi 开始,增重率显著下降(图 1)。在剖检(10、20、30 dpi)时,严重的胸腺萎缩、轻度至中度的脾脏和法氏囊萎缩、骨髓和脾脏苍白以及肝坏死是感染鸭子的常见病变。当比较组织的大小和颜色时发现,病变随着时间的推移而变得更加严重,并且GPV和DuCV共同感染引起的疾病严重程度比单独感染GPV或DuCV更为严重(图2)。组织病理学最主要的病变在肝脏、肾脏、法氏囊、骨髓、脾脏、胸腺和十二指肠。
肝脏:GPV感染组出现局灶性空泡变性、肝细胞坏死和淋巴细胞浸润。在DuCV感染组中观察到肝空泡变性和炎症灶。在混合感染组中,肝空泡变性更严重,大面积肝细胞崩解、结构丢失,并有出血。
肾脏:GPV感染组和DuCV感染组肾小管上皮细胞均出现轻至中度空泡变性,混合感染组肾小管上皮细胞变性严重,坏死、脱落,大量异嗜性粒细胞浸润。
十二指肠:GPV感染组可见绒毛脱落、淋巴细胞浸润,DuCV感染组未见明显病变,混合感染组可见绒毛坏死脱落、出血,腺管上皮细胞萎缩,淋巴细胞浸润。
合并感染组免疫器官(脾脏、胸腺、法氏囊、骨髓)病变较单感染组严重,包括淋巴细胞减少、出血、嗜异性粒细胞浸润,骨髓、胸腺、脾脏组织细胞减少,胸腺小体崩解。
图 2. 感染鸭的大体病变。在 GPV 和 DuCV 共感染组中,它们表现为严重的胸腺萎缩、轻度至中度的脾脏和法氏囊萎缩、骨髓和脾脏苍白以及肝坏死。比例尺=1厘米。
2.2 组织中病毒载量
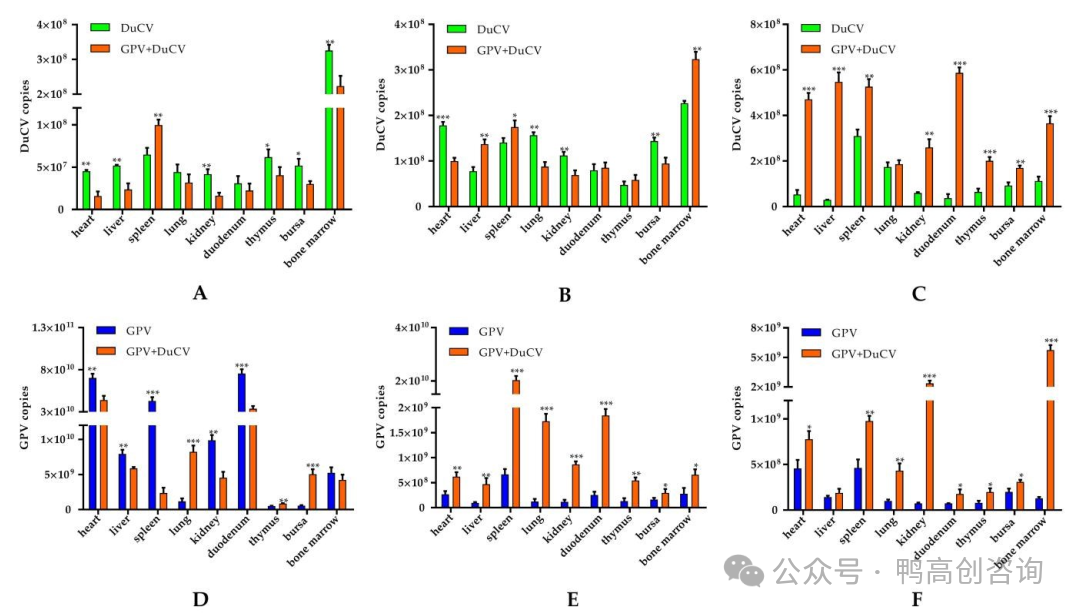
通过qPCR检测不同时间点组织(心脏、肝脏、脾脏、肺脏、肾脏、十二指肠、胸腺、法氏囊和骨髓)中GPV和DuCV载量,观察病毒在体内复制的动态变化。混合感染组的脾脏、肺脏和十二指肠30 dpi水平较20 dpi水平下降(P< 0.001),而在肾脏和骨髓中升高(P< 0.01)。GPV感染组和混合感染组的心脏、肝脏、胸腺和法氏囊中的GPV积累保持在与之前相同的水平。除肝脏外,共感染组组织中GPV含量显著高于GPV单感染组(P < 0.05)(图3F)。感染初期,共感染组DuCV和GPV复制均受到抑制。但随着感染进程的发展,两种病毒的复制在该组织中协同增加,比单独感染的病毒载量更高。
2.3 病毒在鸭组织中的分布
用IHC检测GPV和DuCV在体内的分布和定位,在肝脏、脾脏、肾脏、十二指肠和法氏囊中检测到阳性细胞。随着感染时间延长,肝脏、十二指肠、脾脏阳性细胞数增多,混合感染组阳性细胞数合并感染组在10 dpi和20 dpi的阳性细胞数均低于单一感染组,但在30 dpi时阳性细胞数高于单一感染组;由于淋巴细胞的耗竭,法氏囊内阳性细胞数减少,但信号强度增加。
据报道GPV引起鸭子显著的生长迟缓、厌食和腹泻,而DuCV感染鸭子的症状则以生长迟缓和羽毛脱落为特征。
本研究证明了GPV和DuCV对鸭子具有感染协同作用。与单一感染组相比,混合感染的致病性明显增强,对鸭的生长发育影响更为严重,临床症状和病理改变也更为严重。主要病变为肝脏、肾脏、十二指肠变性、坏死、出血,淋巴细胞浸润,脾脏、胸腺、法氏囊等免疫器官萎缩,骨髓和组织细胞丢失。DuCV和GPV感染的特征性病变均出现,但以免疫器官的病变最严重。肝脏、肾脏作为主要的代谢器官,病变较为严重,病毒载量较高。
此外,本研究显示GPV和DuCV共感染具有协同促进体内复制的作用。在病毒协同作用中,病毒复制、细胞病理改变、组织趋向性、宿主范围以及一种或两种病毒的传播率等生物学性状都发生了改变。
在10 dpi时,GPV和DuCV单感染组的大多数组织中的病毒载量高于共感染组。在30 dpi时,DuCV感染组的DuCV载量降低,而共感染组的DuCV载量继续升高。GPV单感染组的病毒载量显著下降,而共感染组的病毒载量略有下降,且在20和30 dpi均高于单感染组。
10 dpi时,共感染组仅脾脏中的DuCV负荷和胸腺、法氏囊和肺脏中的GPV负荷高于单感染组,说明病毒首先在免疫器官中大量复制并诱发病变。共感染组肺脏中GPV含量持续较高,而DuCV含量不高,说明GPV与DuCV共感染导致血液含量高的组织对GPV更易感,仅增加该病毒的复制。20 dpi时,共感染组的脾脏中GPV病毒载量最高。30 dpi时,骨髓中GPV复制是单感染组的43倍。
DuCV是一种免疫抑制病毒,它削弱宿主的免疫反应,使其易受继发感染。近年来GPV作为SBDS的病原体被广泛研究,但目前实验室感染的成功率仅为20%~35%。针对这一问题,我们在野外调查病例,发现GPV与DuCV在鸭中混合感染率较高,尤其在SBDS中。同样,在观赏鸭中也发现鹅圆环病毒(GoCV)与GPV混合感染,死亡率较高。由于实验室感染与自然感染条件不同,且DuCV与GPV在鸭体内的潜伏期较短,本研究中的鸭子均未发现SBDS症状,但DuCV与GPV表现出协同致病作用。目前对鸭病DuCV与GPV混合感染混合感染的研究较少,DuCV感染的发病机制尚不明确,根据已报道的研究和资料,细胞凋亡可能在圆环病毒感染的发病机制中起重要作用。本研究发现混合感染鸭的脾脏和法氏囊中淋巴细胞数量减少,IHC信号强度增强。GPV和DuCV共感染致病性增强可能是由于DuCV诱导免疫细胞凋亡,导致免疫抑制和生长停滞,使鸭对GPV更敏感,促进病毒在鸭组织中复制,从而加重病情。
GPV和DuCV的混合感染显著抑制了鸭的生长发育,并导致免疫器官萎缩、苍白,肝脏坏死。GPV和DuCV在混合感染的鸭中协同增强了致病性。感染初期,混合感染鸭体内两种病原体的病毒载量显著低于单一感染鸭随着感染进程的进展,混合感染鸭体内GPV和DuCV的载量显著高于单一感染鸭。病毒在肝脏、肾脏、十二指肠、脾脏和法氏囊中的分布范围扩大,与GPV和DuCV混合感染鸭体内病毒载量的增加相一致。结果表明GPV和DuCV在混合感染鸭体内具有协同增强复制和致病性的效应。
参考文献:Liu J , Yang X , Hao X ,et al.Effect of goose parvovirus and duck circovirus coinfection in ducks[J].Journal of Veterinary Research, 2020.DOI:10.2478/jvetres-2020-0048.


